在医疗器械的广阔领域中,根据风险等级实行分类管理是国际通行的科学监管模式。我国依据《医疗器械监督管理条例》及配套的《医疗器械分类目录》,将医疗器械划分为第一类、第二类和第三类,风险程度依次递增。其中,第一类医疗器械作为风险程度最低的类别,构成了医疗健康体系的基础层,其界定、管理与应用直接影响着公众日常健康防护的可及性与安全性。
第一类医疗器械的界定与核心特征
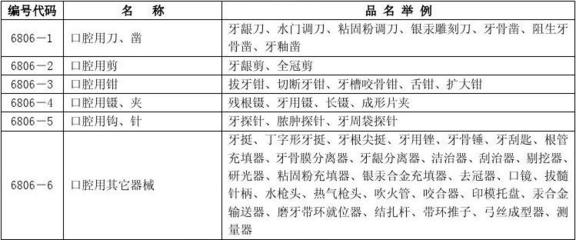
根据《医疗器械分类目录》的核定,第一类医疗器械是指“风险程度低,实行常规管理可以保证其安全、有效的医疗器械”。其核心特征在于“低风险”与“常规管理”。这类产品通常结构简单,作用机理明确,多数不具备药理学、免疫学或代谢学方面的作用,或者仅参与其过程。其安全性主要通过物理方式实现,有效性有长期成熟的使用历史验证,预期用途明确且局限。例如,外科手术中使用的非无菌提供的手术刀、刀片、剪子;病房中常见的病床、轮椅、拐杖、医用冰袋、绷带;以及检查诊断用的诊察器械如压舌板、诊察锤、听诊器(非电子)等,均属于典型的第Ⅰ类医疗器械。它们为诊断、治疗、护理及康复提供了最基础的工具和环境支持。
科学监管:备案制与全过程管理
与风险较高的第二类(注册管理)、第三类(严格注册管理)医疗器械不同,我国对第一类医疗器械的管理实行 “备案制” 。产品备案由备案人向所在地设区的市级人民政府食品药品监督管理部门提交备案资料。备案资料重点包括产品风险分析资料、产品技术要求、产品检验报告、临床评价资料(通常为免于进行临床评价的说明)、生产制造信息及产品说明书标签样稿等。备案过程相对简化,但绝非放松要求。监管部门通过备案建立产品档案,并持续进行上市后监管,包括对生产条件、产品质量的监督检查,不良事件的监测与再评价,确保产品在全生命周期内持续符合安全有效的基本要求。这种“宽进严管”的模式,既鼓励了产业创新与供应,又牢牢守住了安全底线。
广泛应用:渗透于医疗与日常保健的各个角落
第一类医疗器械的应用场景极为广泛,几乎渗透到从专业医疗机构到家庭日常保健的每一个环节:
- 医院临床基础操作:如清创缝合用的基础外科器械、固定骨折用的医用夹板、普通护理用的各种器具。
- 物理康复与辅助:如康复训练器械、助行器、矫形器等(非植入、非活性)。
- 检查与诊断辅助:如医生使用的传统诊察工具、身高体重测量设备等。
- 家庭与个人护理:这是与公众联系最紧密的领域,包括医用棉签、纱布、一次性医用口罩、医用冷敷贴、避孕套等。这些产品在药店、电商平台随处可见,是人们进行自我健康管理的第一道工具。
产业意义与公众认知
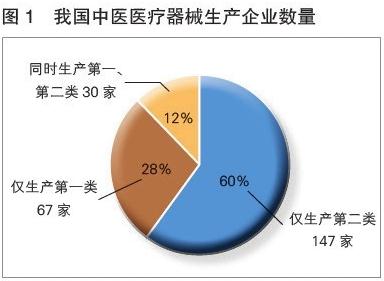
第一类医疗器械产业是医疗器械行业的基石。其技术门槛相对较低,企业数量众多,产品种类丰富,在保障基础医疗供给、降低医疗成本、促进基层医疗卫生服务能力方面发挥着不可替代的作用。它也是许多医疗器械企业入行发展的起点。
对于公众而言,正确识别和合理使用第一类医疗器械至关重要。消费者应通过正规渠道购买已备案的产品,注意查看产品包装上是否标有医疗器械备案凭证编号(格式通常为“×械备××××××××”),并严格按照说明书使用。尽管风险较低,但错误使用或使用不合格产品仍可能带来健康风险。例如,使用无菌要求不达标的外科敷料可能导致感染,使用设计不合理的矫形支具可能加重损伤。
与展望
《医疗器械分类目录》核定的第一类医疗器械,是建立在科学风险评价基础上的、通过备案制实施监管的低风险医疗产品。它们构成了医疗健康保障体系的“毛细血管”,支撑着从专业诊疗到家庭保健的广泛需求。随着科技进步和健康意识的提升,第一类医疗器械的产品边界也在动态调整,一些新型低风险产品可能被纳入,而部分产品也可能随着风险认知的深入被重新分类。在持续优化备案流程、加强事中事后监管、提升公众用械安全意识的第一类医疗器械将继续以其基础而关键的角色,守护人民群众的生命健康与生活质量。