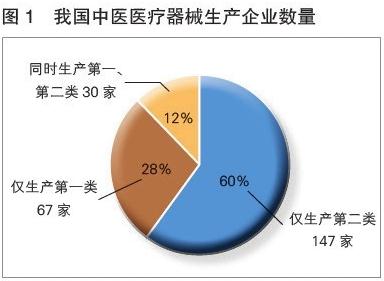
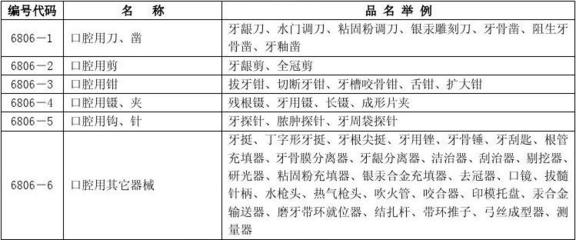
第一类医疗器械是指风险程度低,实行常规管理可以保证其安全、有效的医疗器械。根据《医疗器械监督管理条例》规定,第一类医疗器械产品备案与生产备案是相关企业进入市场前必须完成的关键环节。本文将系统阐述备案所需资料的具体要求及相关说明,以帮助企业高效、合规地完成备案工作。
一、 第一类医疗器械产品备案资料要求
产品备案,即对拟上市的第一类医疗器械产品进行信息登记。申请人(备案人)需向所在地设区的市级人民政府负责药品监督管理的部门提交以下资料:
- 第一类医疗器械备案表:需在线填报并打印,内容应完整、准确,包括产品名称、分类编码、型号规格、预期用途、备案人及生产地址等信息。
- 安全风险分析报告:应按照YY/T 0316《医疗器械风险管理对医疗器械的应用》标准的要求编制,详述产品在正常和故障状态下的已知和可预见的风险,以及所采取的风险控制措施。
- 产品技术要求:应按照《医疗器械产品技术要求编写指导原则》制定,明确产品性能指标和检验方法。内容应清晰、完整,用语规范。
- 产品检验报告:可以是备案人的自检报告,也可以是委托有资质的医疗器械检验机构出具的检验报告。报告应能证明产品符合技术要求。
- 临床评价资料:根据《医疗器械临床评价技术指导原则》,第一类医疗器械通常可免于进行临床试验,通过同品种比对等方式提交临床评价资料,证明产品安全有效。
- 产品说明书及最小销售单元标签设计样稿:应符合《医疗器械说明书和标签管理规定》的要求,内容真实、完整、准确。
- 生产制造信息:包括产品生产工艺过程及控制点、主要生产设备和检验设备清单等,以证明具备持续稳定生产合格产品的能力。
- 证明性文件:包括企业营业执照副本复印件、备案人出具的真实性声明等。
- 符合性声明:声明所提交备案资料的真实性,以及产品符合现行国家标准、行业标准或备案产品技术要求的声明。
二、 第一类医疗器械生产备案资料要求
生产备案,是对从事第一类医疗器械生产活动的企业进行条件登记。申请人应向所在地设区的市级人民政府负责药品监督管理的部门提交:
- 第一类医疗器械生产备案表。
- 所生产产品的医疗器械备案凭证复印件(已完成产品备案)。
- 企业组织机构图及人员资质证明(如生产、技术和质量负责人的身份、学历、职称证明复印件)。
- 生产、质量和技术岗位人员的从业资质、培训记录等。
- 生产场地证明文件(如产权证明、租赁协议复印件)。
- 主要生产设备和检验设备目录。
- 质量手册和程序文件目录,证明已建立符合《医疗器械生产质量管理规范》要求的质量管理体系。
- 生产工艺流程图。
- 证明性文件(如营业执照副本复印件)。
- 真实性声明,对所提交资料的真实性负责。
三、 重要事项说明
- 备案性质:第一类医疗器械备案是告知性备案,不是行政许可。监管部门对提交的资料进行形式审查,符合要求的即予备案,发放备案凭证。但备案后,备案人需对备案资料的真实性、合规性及产品质量负全部责任。
- 变更与取消:备案信息发生变化(如产品名称、型号规格、预期用途发生实质性变化,或备案人名称、住所变更),应主动向原备案部门申请变更备案。产品不再生产的,应申请取消备案。
- 资料形式:所有资料均需加盖企业公章。鼓励通过在线政务服务平台提交电子资料,提高办理效率。
- 属地管理:备案工作遵循属地管理原则,应向备案人/生产企业所在地的市级监管部门提出申请。
- 合规基础:完成备案仅是第一步,企业必须持续遵守《医疗器械监督管理条例》及配套规章,确保生产活动全过程符合医疗器械生产质量管理规范的要求,保障产品质量安全有效。
第一类医疗器械备案工作系统而具体。企业应充分理解法规要求,严谨准备备案资料,确保内容真实、准确、完整,从而顺利通过备案,为产品的合法上市与企业的规范运营奠定坚实基础。